日本科学家重建“体外卵巢”,成功制造卵子
本周的《科学》杂志上,日本的科研人员带来了干细胞领域的一项新突破。他们用小鼠胚胎干细胞,制造出了卵母细胞成熟所需的结构——卵巢中的卵泡。在干细胞制造的“体外卵泡”中,原始生殖细胞得以生成具有完整功能的卵子,这些卵子最终受精并孕育出了健康的小鼠后代。
《科学》评论:“这项技术突破激发了生殖细胞研究的巨大潜力。”

在体外制造人类的生殖细胞,一直是生殖生物学家所追求的目标。先前,人们在制造原始生殖细胞(产生雄性和雌性生殖细胞的早期细胞)方面已经取得了一些进展。在过去的研究中,科学家们已经可以使用小鼠的胚胎干细胞造出卵母细胞,也就是卵子的前体。
但这些前体细胞必须移植回雌性动物体内,或者从动物体内分离出卵巢细胞,才能进一步产生卵子。这是因为,卵母细胞需要在一个充满液体的特殊囊泡中成熟。这个囊泡叫做卵泡,组成卵泡的体细胞提供了多种营养成分和信号分子,支持卵母细胞的生长和分裂。
“如何诱导卵母细胞成为功能成熟的卵细胞,成为体外配子发生的一个关键问题,也是重要挑战。”此次研究的作者在论文中指出。
 在这项新研究中,九州大学的科研人员成功创建了可供卵子发育的卵泡结构,让干细胞制造的卵母细胞可以在体外发育成熟。研究小组开发了一套培养条件,通过在不同时间点提供不同的信息分子,诱导雌性小鼠的胚胎干细胞逐步分化,最终产生了大量与卵巢体细胞类似的细胞。他们将其命名为胚胎卵巢体细胞样细胞(简称FOSLC)。
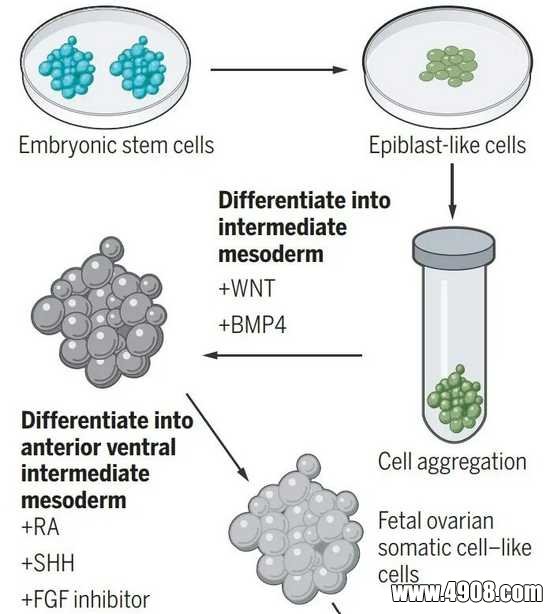
当这些FOSLC与来自小鼠胚胎干细胞的卵母细胞(被称为原始生殖细胞样细胞,简称PGCLC)放在一起共同培养时,FOSLC产生了卵巢卵泡结构,而PGCLC在里面发育成有活力的卵子。
更可喜的,这些体外生成的卵子完全具有该有的功能:它们可以受精,受精卵产生的胚胎移植到雌性小鼠子宫内,产生了健康、有生育能力的后代。
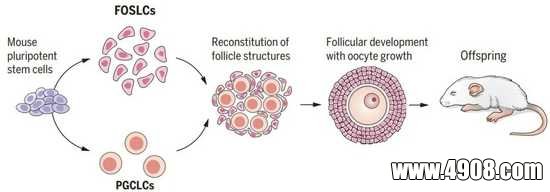 研究人员总结说,这项技术为体外大规模产生卵子提供了一个模型系统,这可能对辅助生殖技术产生影响。
但《科学》同时发表的评论也指出,这项技术如果要进一步运用于人类,可能会带来一些伦理上的担忧。在技术逐渐成熟的同时,考虑任何临床应用并最终实现之前,科学界和公众都必须非常谨慎,监管也应跟上技术的步伐,以免出现伦理上的灾难。
参考资料: [1] Takashi Yoshino et al。, (2021) Generationof ovarian follicles from mouse pluripotent stem cells。 Science Doi: 10.1126/science.abe0237 [2] Lin Yang and Huck-Hui Ng (2021) Themaking of an ovarian niche。 Science Doi: 10.1126/science.abj8347 |
- “宇宙磁体”制造又有新方法
- 科学家称:基于等离子体技术可制造火星氧气
- 日媒:日本专家在猴子身上成功试验艾滋病疫
- 中国科大陈秀雄团队成功证明凯勒几何两大核
- 为什么人类卵子的体积是精子的上千万倍?
- 科学家成功在猪的淋巴结上培植出备用肝脏
- 揭示银河系反物质来源:每秒钟制造9万亿千
 |
咖啡和茶可降低中风、痴呆症发病 |
| 每天喝2-3杯咖啡或3-5杯茶,或者同时喝4-6杯茶或咖啡 |
 |
南越王宫千年古井仍有活水 |
| 摘要:备受关注的南越王宫博物馆,又再掀起一角面纱。 |
- 发表评论
-
- 最新评论 进入详细评论页>>